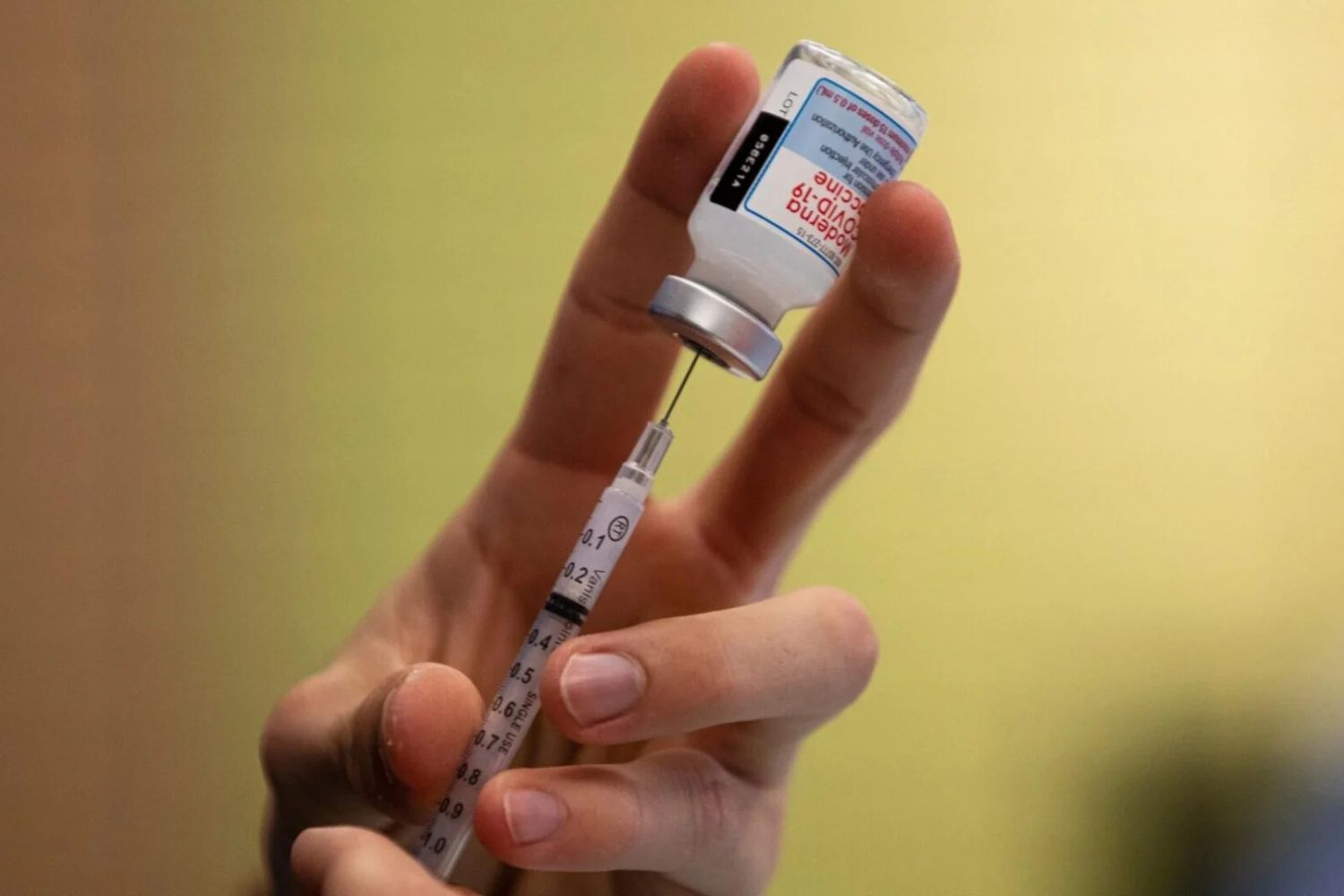
El gobierno federal parece no ser amigo de las vacunas, y ahora hay una nueva demostración de eso porque la FDA (Agencia de Drogas y Alimentos) se ha negado a revistar la prometedora vacuna antigripal experimental con ARN mensajero de Moderna, que solicitó su aprobación.
Moderna reveló la negativa de la FDA el martes por la noche, al postear la carta de rechazo en línea. Allí, con la firma del funcionario Vinay Prasad, la FDA afirma que los datos del ensayo en Fase III de Moderna no incluían un grupo de control adecuado para comparación. Moderna declaró que había seguido las recomendaciones previamente acordadas con la agencia. Pero aparentemente Prasad decidió unilateralmente rechazar la solicitud de Moderna, a pesar de las objeciones de los científicos de la FDA.
La decisión de la FDA “que no identificó objeciones por eficacia ni seguridad, no acompaña el esfuerzo por el objetivo compartido de mejorar y realzar el liderazgo de EE.UU. en el desarrollo de medicinas innovadoras”, declaró el CEO de Moderna Stéphane Bancel.
Sin problemas de seguridad
La compañía publicó los datos de la Fase III de su vacuna estacional contra la gripe, con nombre en código MRNA-1010, en marzo. El ensayo incluyó a casi 10.000 participantes. Como mínimo, la vacuna demostró ser segura y efectiva como vacuna antigripal de rigor para adultos menores de 65, y como vacuna de más alta dosis para adultos mayores de 65. Basándose en los niveles de anticuerpos la mRNA-1010 incluso brindaría mayor protección que las típicas vacunas antigripales. Los autores del trabajo de investigación dijeron que “no encontraron problemas de seguridad”.
Pero en la carta de Prasad a Moderna, emitida la semana pasada, afirma que los grupos de control que usó Moderna “no reflejan los mejores parámetros disponibles de cuidado”. La carta no define cuáles serían esos parámetros. Y Moderna, en su respuesta, declaró que el CEBR le había dado el visto bueno al protocolo propuesto por la compañía para su mayor ensayo en Fase III de la mRNA-1010 en 2024. La agencia recomendó que Moderna incluyera un grupo de comparación de adultos mayores de 65 años a quienes se aplicara la vacuna antigripal de alta dosis. La compañía ya había llevado a cabo ensayos más pequeños en Fase III y en uno de ellos había incluido esa comparación, presentando los datos en su solicitud ante la FDA el año pasado (los datos se incluyeron en el estudio mencionado más arriba).
La compañía dice que la FDA no dijo en ningún momento que no estuvieran satisfechos con la calidad de los datos de Moderna, antes de rechazar la solicitud. Parece que en tiempos normales la FDA al menos habría considerado la vacuna de Moderna para su aprobación. Citando a tres funcionarios anónimos de la FDA, Stat News informó el miércoles que Prasad, jefe del Centro de Evaluación e Investigación Biológica de la FDA (CBER) no consultó con su personal y decidió rechazar de plano la solicitud de la compañía.
Encono contra el ARN mensajero
El rechazo de la FDA es el más reciente en reflejar la animosidad reciente del gobierno hacia la tecnología del ARN mensajero. Eso empezó en el segundo gobierno de Trump y la designación de Robert F. Kennedy Jr. como jefe del Departamento de Salud y Servicios Humanos.
Prasad fue nombrado jefe del CBER en mayo del año pasado, y fue despedido en julio, pero lo recontrataron menos de dos semanas después. También ha mostrado dudas sobre la efectividad y seguridad de las vacunas de ARN mensajero contra el COVID. Dijo ante miembros de la FDA que esas vacunas habían causado la muerte de al menos diez niños en EE.UU., citando un análisis no publicado de la FDA. Esos datos no se han publicado, pero poco después se filtró un memo interno que indica que los científicos de la FDA encontraron menos muertos vinculados a las vacunas (posiblemente, cero).
También, Prasad y otros funcionarios han dicho que la FDA requerirá evidencia más rigurosa para la aprobación de vacunas en el futuro. Es una idea lógica en teoría pero en la práctica podría exigir ensayos controlados por placebo para enfermedades que ya tienen vacunas, ensayos que no serían éticos porque expondrían a algunos voluntarios a enfermedades prevenibles, según muchos expertos.
Es probable que como resultado de este escrutinio más riguroso Moderna demorara su solicitud de aprobación para una vacuna combinada de ARN mensajero, contra la gripe y el COVID, que el año pasado parecía prometedora. Moderna dijo que necesitaba recoger más datos. Su vacuna mRNA-1010 está siendo evaluada para su aprobación en otros países, como Canadá y la Unión Europea. Moderna ha dicho que pidió una reunión con el CBER para entender mejor la decisión de la agencia.
Toda esta saga podría ilustrar que si uno intenta jugar según las reglas actuales de la FDA, es probable que pierda la batalla.