Los medicamentos Wegovy y similares para bajar de peso pueden causar más efectos secundarios de los actualmente reconocidos. La Administración de Alimentos y Medicamentos está investigando ahora si estos Los medicamentos contra la obesidad de nueva generación pueden provocar pérdida de cabello, ideas suicidas y aspiración de alimentos, según informes de eventos adversos relacionados con su uso. Los informes solo pretenden ser una posible señal de advertencia y no prueban la causalidad, pero la FDA podría tomar medidas regulatorias adicionales en caso de sus investigaciones dan frutos, como la modificación del etiquetado de los medicamentos.
La FDA mantiene una lista pública de posibles nuevos riesgos de seguridad asociados con los medicamentos aprobados, basada en los informes enviados a la FDA de eventos adversos. Sistema de informes (FAERS). En una actualización liberado El martes, que abarca de julio a septiembre de 2023, la agencia actualmente está señalando un vínculo potencial entre las drogas GLP-1 y las ideas suicidas, la alopecia (pelo pérdida ) y aspiración (el riesgo de que los alimentos pasen por nuestras vías respiratorias y pulmones, lo que puede causar problemas como neumonía). Para cada uno de Ante estas posibles preocupaciones, la FDA afirma que está “evaluando la necesidad de tomar medidas regulatorias”.
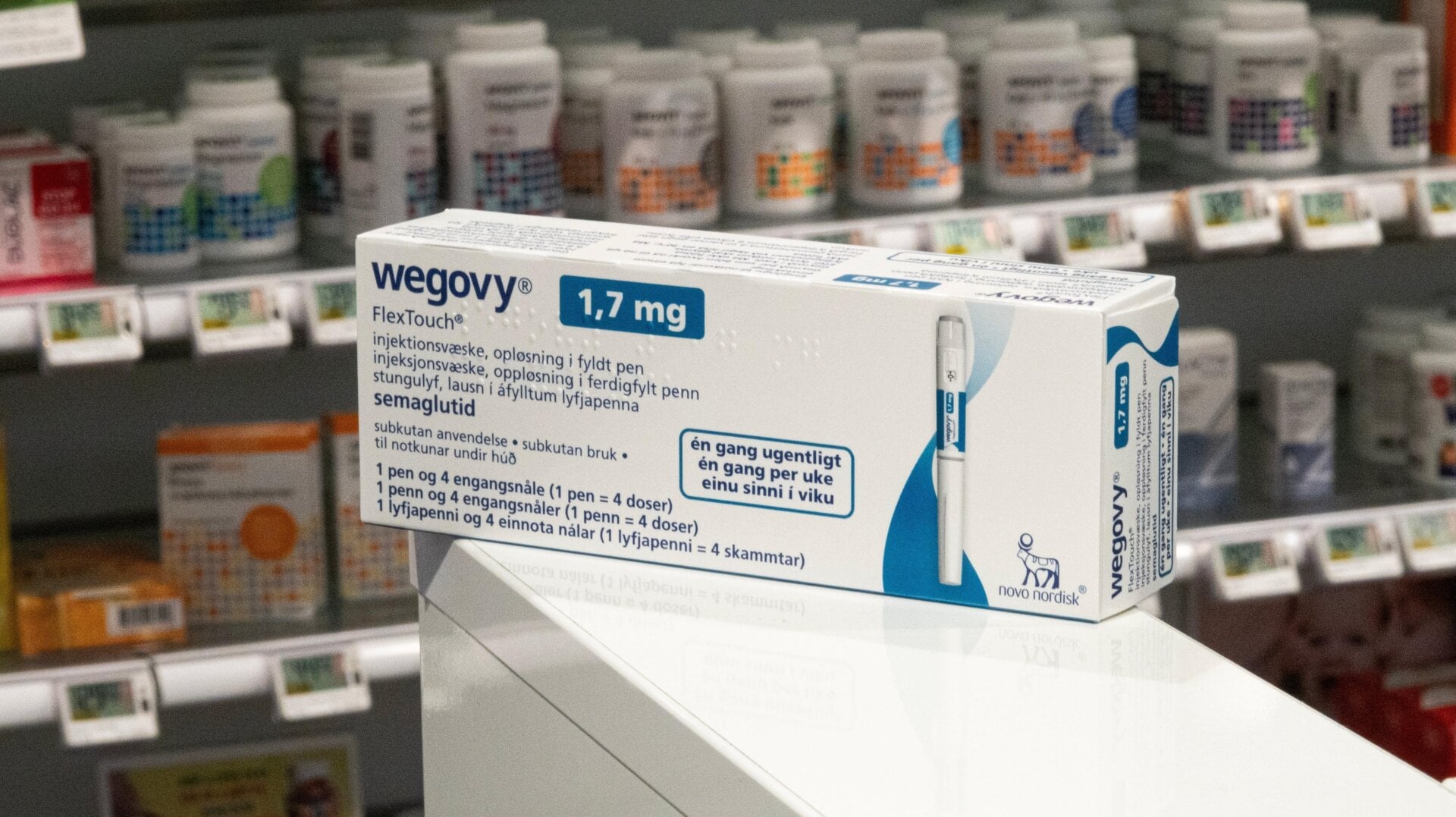
Wegovy pertenece a una clase de fármacos conocidos como incretinas, llamados así por un grupo de hormonas que ayudan a regular nuestro metabolismo y el hambre. El ingrediente activo es la semaglutida, una versión sintética y más duradera de la hormona GLP-1. En 2017, Novo Nordisk recibió la aprobación de la FDA para su Ozempic, un medicamento para la diabetes tipo 2, también elaborado con semaglutida; en 2021, la compañía obtuvo la aprobación para una versión de dosis más alta bajo el nombre Wegovy, destinado explícitamente, a tratar la obesidad. En 2022, Eli Lilly obtuvo la aprobación de su fármaco de incretina similar, Mounjaro, elaborado con el ingrediente activo tirzepatida, para tratar la diabetes tipo 2 (tirzepatida imita GLP-1 y otra hormona incretina llamada GIP). Y este otoño, Eli Lilly recibió aprobación para un medicamento contra la obesidad a base de tirzepatida vendido bajo la marca Zepbound.
Como sea que los llames, estos medicamentos tienen cambiado dramáticamente El panorama del tratamiento de la obesidad desde su llegada. En ensayos clínicos, han ayudado a las personas a perder sustancialmente más peso que la dieta y el ejercicio solos. . Superan a los medicamentos más antiguos para la obesidad, y los pacientes pierden del 15% al 25% de su peso inicial en un año de un año. Hasta ahora, Los medicamentos parecen ser en general seguros y tolerables, y los efectos secundarios más comunes documentados en los ensayos son síntomas gastrointestinales como náuseas y vómitos. y estreñimiento, que puede disminuir con el tiempo.
Pero tras la aprobación de estos medicamentos, algunos pacientes y médicos han informado complicaciones más graves Posiblemente ligado a su uso. Estas complicaciones han incluido gastroparesia (parálisis estomacal), pancreatitis e íleo (obstrucción intestinal), entre otras.
En septiembre de 2023, basándose en estos informes, la FDA actualizado su etiquetado de Wegovy y Ozempic, advirtiendo que los productos podrían potencialmente causar íleo, aunque la agencia no confirmó como un efecto establecido riesgo. El año pasado, los reguladores sanitarios de Islandia, el Reino Unido y, finalmente, la Unión Europea anunciadoque comenzarían a investigar un vínculo potencial entre la idea de suicidio y el uso de GLP-1 después de los informes de casos. Y ahora la FDA ha siguió su ejemplo.
Como la FDA tiene cuidado de señalar en su sitio web, los informes de eventos adversos no deben ni pueden usarse para demostrar que un La droga causa un problema particular y tampoco se pueden usar para estimar qué tan común podría ser un riesgo potencial para la seguridad. Como ejemplo, Algunos síntomas, como la caída del cabello, tienen muchas causas, por lo que una persona que pierde el cabello mientras toma un medicamento GLP-1 puede haberlo hecho. entonces, si estaban tomando el medicamento o no. Algunos expertos también han notado un falta de evidencia vinculando el uso de GLP-1 con el riesgo de suicidio en ensayos clínicos, en los que han participado colectivamente miles de personas.
Al mismo tiempo, los datos sobre eventos adversos son una valiosa fuente de información, y se han descubierto efectos secundarios previamente desconocidos de los medicamentos. estos informes iniciales. Por lo tanto, estas investigaciones de la FDA y otras agencias de salud podrían muy bien conducir a acciones regulatorias. Estas acciones probablemente incluir cambios adicionales en el etiquetado de estos medicamentos. Pero no es sin precedentes que los reguladores promulguen medidas más estrictas, como la caja negra. advertencias o incluso retirar directamente un medicamento del mercado. Esto último probablemente sólo sucedería si algún efecto secundario recientemente descubierto contrarresta claramente la Sin embargo, los beneficios conocidos de estos medicamentos, que parecen extenderse más allá pérdida de peso sola.