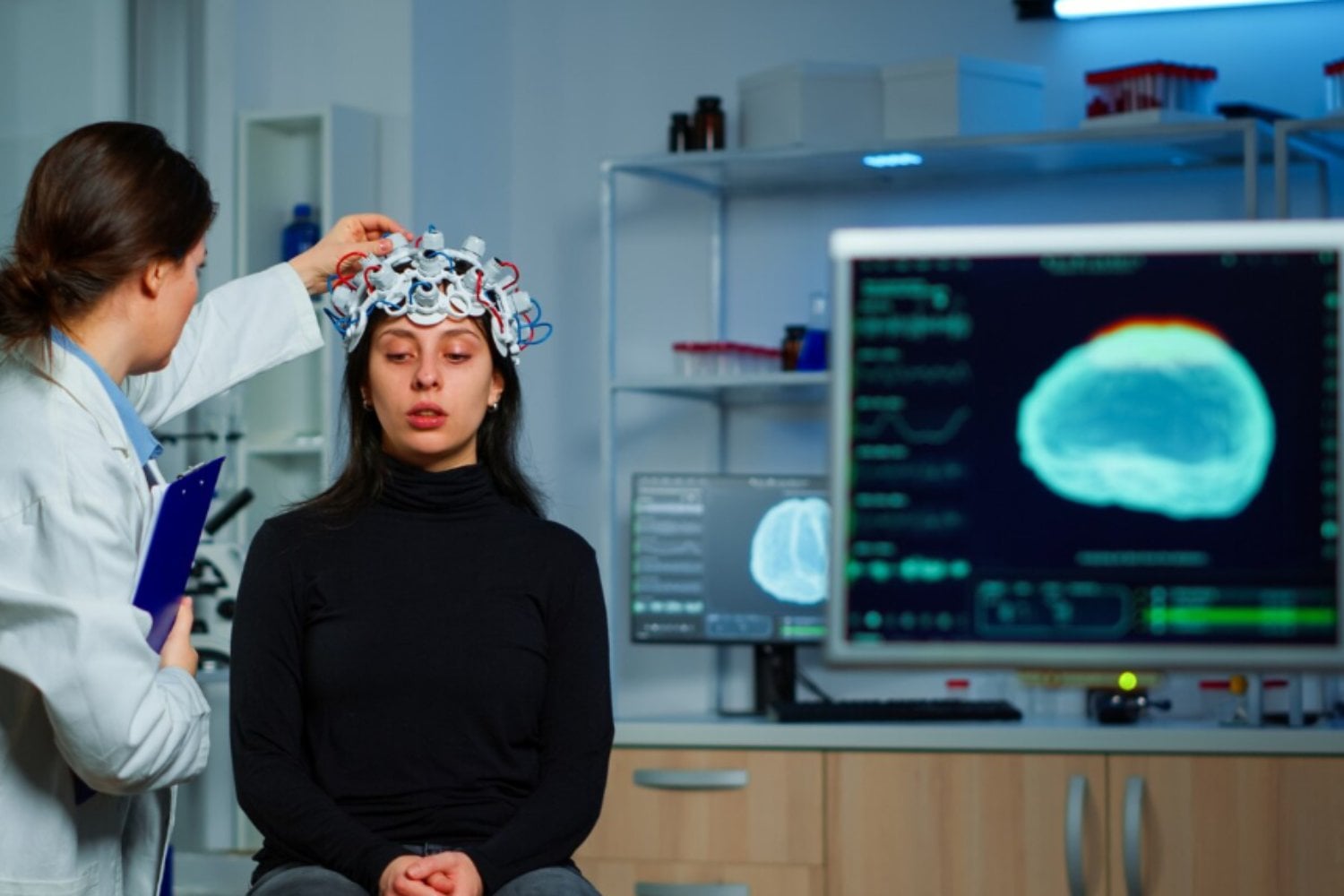
Un minuto. Eso es lo que tarda un ictus en alterar para siempre la vida de una persona. Un vaso sanguíneo se obstruye, el flujo de oxígeno se interrumpe y miles de neuronas mueren en cuestión de segundos. Aunque la medicina moderna ha aprendido a salvar a muchos pacientes, el cerebro dañado no suele recuperarse por completo.
Pero ese límite podría estar a punto de cambiar. En los últimos años, las terapias con células madre han abierto una vía prometedora para reparar el tejido cerebral tras un ictus. Por primera vez, la idea de regenerar un cerebro lesionado empieza a dejar de ser ciencia ficción.
Un órgano brillante… y frágil
El cerebro es el centro de control más complejo conocido. Coordina el pensamiento, la memoria, el lenguaje, las emociones y el movimiento. Pero, paradójicamente, su capacidad de regeneración es mínima.
A diferencia del hígado o la piel, las neuronas que mueren rara vez se reemplazan. Por eso, lesiones como las provocadas por un ictus suelen dejar secuelas motoras, cognitivas o emocionales que acompañan al paciente toda la vida.
El ictus isquémico, causado por la obstrucción del flujo sanguíneo hacia una parte del cerebro, es una de las principales causas de discapacidad en adultos. Aunque los tratamientos de emergencia han mejorado la supervivencia, no existe aún una terapia capaz de reconstruir el tejido neuronal destruido.
La rehabilitación ayuda a recuperar parte de la función, pero en muchos casos los pacientes quedan con limitaciones permanentes. Aquí es donde entra en juego la medicina regenerativa.

Células madre: reparar lo irreparable
Las terapias con células madre buscan reemplazar las células muertas o dañadas por otras nuevas capaces de integrarse en el tejido afectado y restaurar sus funciones. En el caso del cerebro, el objetivo es que las nuevas neuronas no solo sobrevivan, sino que formen conexiones funcionales con las que quedaron intactas.
Este enfoque tiene antecedentes históricos. En la década de 1980, los neurocientíficos Anders Björklund y Olle Lindvall, del Hospital Universitario de Lund (Suecia), trasplantaron células madre neurales en pacientes con Parkinson.
El resultado fue asombroso: muchos recuperaron la función motora durante más de una década. Fue la primera evidencia real de que el cerebro humano puede ser reparado con células vivas.
Desde entonces, los ensayos clínicos se han multiplicado y la regulación europea ha establecido normas para garantizar la seguridad de estas terapias, ahora clasificadas como Medicamentos de Terapia Avanzada (ATMP). Sin embargo, aplicar esta idea al ictus presenta desafíos más complejos.
El reto del cerebro dañado por un ictus
A diferencia del Parkinson, que afecta a un tipo de neuronas muy específico, el ictus daña áreas más amplias y heterogéneas: neuronas, glía, vasos sanguíneos y redes completas de conexión.
Por eso, tras un trasplante, no basta con que las células sobrevivan: deben integrarse en el tejido, enviar prolongaciones (axones), recibir señales, crear sinapsis y reconectarse con los circuitos originales. Es como reconstruir un puente… y reactivar el tráfico que lo cruza.
La clave no está solo en añadir células nuevas, sino en restablecer la comunicación neuronal. Y para lograrlo, la biotecnología ha encontrado un nuevo aliado: la ingeniería genética.
Ingeniería genética: neuronas mejoradas
Hoy, los investigadores utilizan modificaciones genéticas de precisión para potenciar la capacidad de las células madre. En algunos laboratorios, se insertan genes como el BDNF (Brain-Derived Neurotrophic Factor), una proteína que estimula el crecimiento neuronal y la formación de sinapsis.
El objetivo es que las células trasplantadas no solo rellenen un hueco, sino que realmente restauren la función cerebral perdida.
Este tipo de ingeniería convierte cada célula en una herramienta inteligente capaz de adaptarse al entorno del cerebro dañado. Sin embargo, también abre debates éticos: ¿hasta dónde se puede —o se debe— modificar una célula humana?
Ciencia y ética: una frontera delicada
Las primeras terapias neuronales usaban tejido fetal, lo que generó controversia. Pero el panorama cambió radicalmente en 2012, cuando el científico japonés Shinya Yamanaka recibió el Nobel por descubrir las células madre pluripotentes inducidas (iPS).
Estas células se obtienen a partir de tejidos adultos —como la piel— y pueden reprogramarse para convertirse en cualquier tipo celular, incluidas neuronas.
Gracias a este avance, es posible crear células madre a partir del propio paciente, evitando el rechazo inmunológico y los dilemas éticos del uso de embriones.
Hoy, la pregunta ya no es si podemos modificar células para curar el cerebro, sino cómo hacerlo con responsabilidad, seguridad y equidad.
El futuro de la regeneración cerebral
Cada ensayo clínico aporta un paso más hacia una medicina verdaderamente reparadora. La combinación de células madre, ingeniería genética y neurociencia está delineando un horizonte en el que los cerebros dañados podrían volver a funcionar.
Aún faltan años para que estas terapias estén disponibles de forma generalizada, pero la dirección es clara: el cerebro no es un órgano irrecuperable.
Como escribió Björklund, pionero de esta revolución, “si el cerebro puede aprender, también puede repararse”.
Fuente: TheConversation.