La resistencia a los antibióticos avanza más rápido que nuestra capacidad para probar nuevos fármacos. En ese cuello de botella, los modelos animales tradicionales se han convertido en una limitación: caros, lentos y cargados de dilemas éticos. La sorpresa llega desde un rincón inesperado del laboratorio: una larva de polilla que, tras ser modificada genéticamente, se comporta como un panel de control biológico que avisa cuándo una infección empeora y cuándo un tratamiento empieza a funcionar.
Un “semáforo” que delata la infección

El truco consiste en introducir genes que hacen que el organismo emita fluorescencia cuando su sistema inmune se activa frente a un patógeno. Bajo el microscopio, las larvas literalmente “se encienden” cuando la infección progresa y “se apagan” cuando el antibiótico logra frenarla. No hay que esperar días para ver si el animal empeora o mejora: la señal es visual y casi inmediata.
Este enfoque convierte a cada larva en un biosensor, según el estudio publicado en Nature. No sustituye a los modelos mamíferos en todas las etapas del desarrollo de fármacos, pero permite un cribado rápido de cientos de compuestos para descartar los que no funcionan o son tóxicos antes de pasar a pruebas más complejas.
Ingeniería genética al servicio del cribado masivo
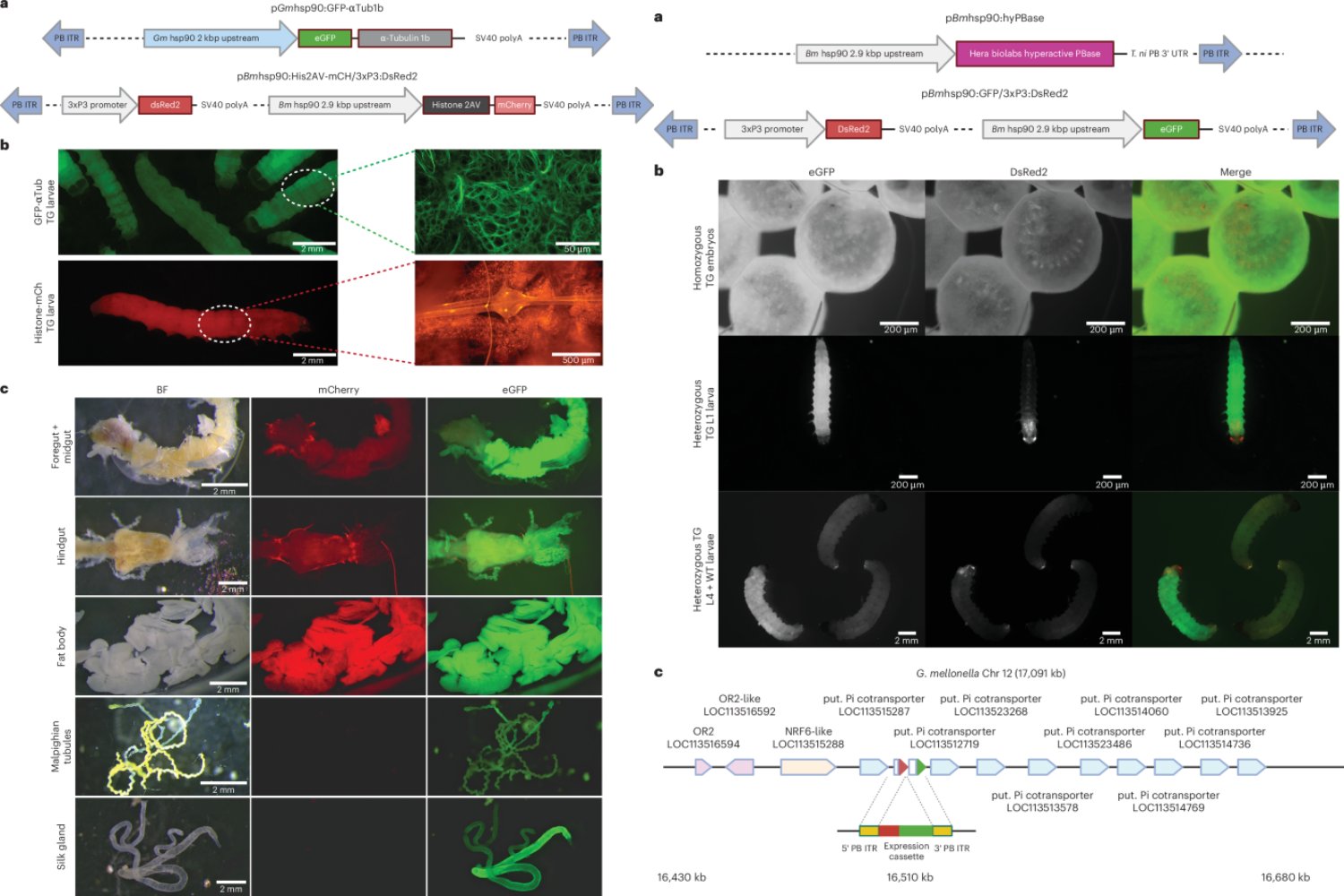
La innovación no está solo en usar insectos, sino en cómo se los ha modificado. Por un lado, se emplean sistemas de inserción genética para que las larvas expresen proteínas fluorescentes asociadas a la respuesta inmunitaria. Por otro, la edición de genes específicos permite “ajustar” su sistema inmune y simular distintos escenarios de vulnerabilidad frente a bacterias u hongos.
Esta combinación hace posible algo que hasta ahora era difícil en modelos invertebrados: observar en vivo la dinámica de una infección y la respuesta a un tratamiento, sin recurrir a técnicas invasivas o a tiempos de espera largos. Es un salto de precisión para un organismo que, hasta hace poco, se consideraba un sustituto tosco del ratón.
Por qué una polilla puede parecerse más de lo que crees
A primera vista, comparar un insecto con un mamífero parece forzado. Sin embargo, la larva de la polilla de la cera tiene dos ventajas prácticas. La primera es que puede mantenerse a 37 °C, la temperatura del cuerpo humano, lo que permite estudiar patógenos que solo activan sus mecanismos de virulencia a esa temperatura. La segunda es que su sistema inmune innato comparte principios básicos con el de los mamíferos: células fagocíticas, respuesta inflamatoria y mecanismos de defensa conservados evolutivamente.
Eso no la convierte en un “ratón barato”, pero sí en un filtro eficaz para decidir qué compuestos merecen llegar a fases posteriores de investigación. En un contexto de emergencia por la resistencia antimicrobiana, ese filtro ahorra tiempo, dinero y animales.
Una respuesta pragmática a una urgencia global
La carrera contra las superbacterias exige probar miles de moléculas en plazos cada vez más cortos. Hacerlo directamente en mamíferos es inviable por costes y por consideraciones éticas. El modelo de las larvas fluorescentes no pretende reemplazar por completo a los ratones, sino aliviar la presión en las primeras fases del desarrollo de fármacos.
A veces, los grandes cambios en el laboratorio no llegan con nuevos robots ni con superordenadores, sino con organismos inesperados que se convierten en herramientas de precisión. Convertir una polilla en un “semáforo” de la infección no resuelve la crisis de los antibióticos, pero introduce algo que la investigación llevaba tiempo necesitando: velocidad para decidir, sin sacrificar rigor ni multiplicar el uso de animales.