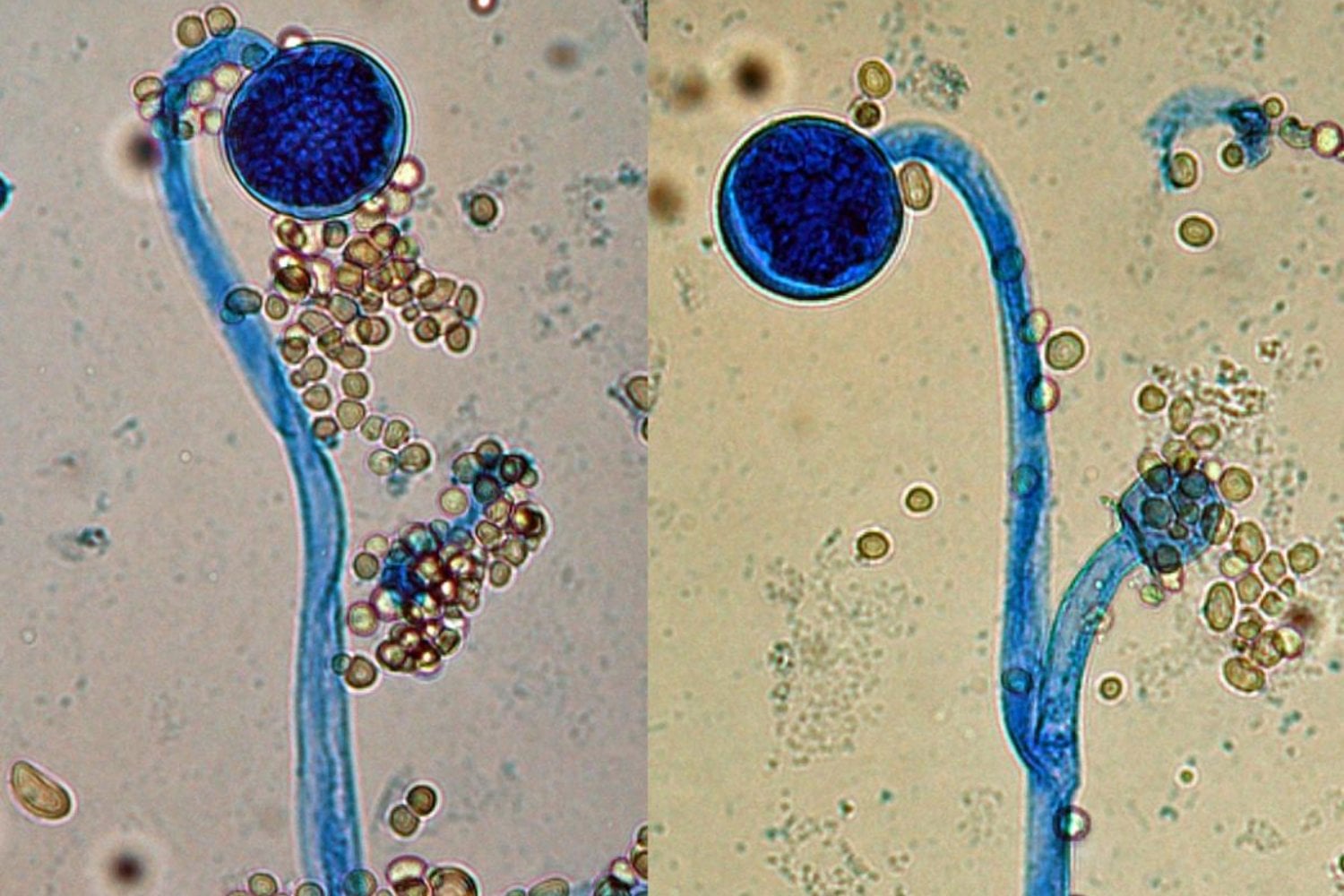
Un organismo que vive descomponiendo hojas muertas puede, en cuestión de horas, convertirse en un invasor capaz de penetrar vasos sanguíneos humanos. No cambia de especie. No adquiere nuevos genes en ese instante. Lo que cambia es el programa que ejecuta.
Esa es la clave del hallazgo liderado por la Universidad de Murcia y publicado en Nature Communications: algunos hongos no se “adaptan” al huésped por accidente. Se reconfiguran.
El rompecabezas del dimorfismo: dos vidas en un solo genoma
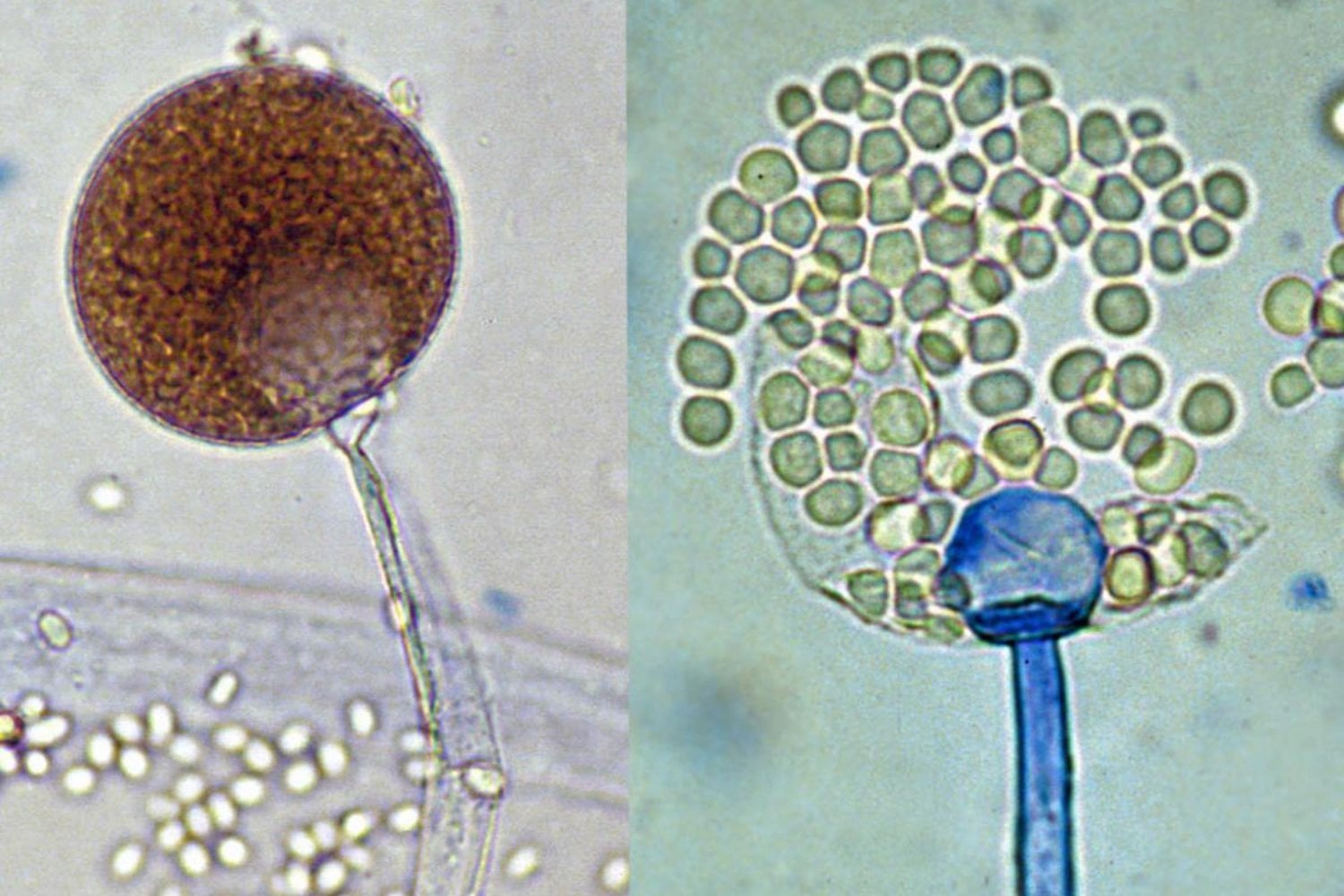
Algunas especies del orden Mucorales, como Mucor lusitanicus, viven tranquilamente descomponiendo materia orgánica en el suelo. Sin embargo, cuando encuentran un huésped vulnerable, pueden cambiar radicalmente su morfología: del micelio filamentoso pasan a una forma de levadura adaptada a invadir vasos sanguíneos. Ese fenómeno se conoce como dimorfismo.
Durante décadas sabíamos que ocurría. Lo que no sabíamos era cómo. El equipo liderado por Francisco E. Nicolás y Victoriano Garre ha demostrado que este cambio no es una reacción improvisada, sino el resultado de una evolución coordinada de familias de genes duplicados. Estos “genes hermanos” (parálogos) se especializaron con el tiempo: unos se activan en la fase ambiental, otros en la fase infecciosa.
El hallazgo más llamativo es la existencia de estructuras genéticas “head-to-head”: pares de genes que comparten región regulatoria y coordinan su expresión dependiendo del entorno. Es un sistema de control fino, casi quirúrgico.
dkl y dfl: los verdaderos arquitectos de la virulencia
Aquí entra en escena el descubrimiento clave. Los genes dkl y dfl no son simples piezas del engranaje: son los reguladores que integran señales ambientales y deciden qué identidad debe adoptar el hongo. Cuando los investigadores desactivaron experimentalmente estos genes, ocurrió algo revelador: el hongo perdió por completo su capacidad de alternar entre formas. Sin dimorfismo, no hay infección eficaz.
Eso significa que la virulencia no depende solo de toxinas o crecimiento rápido, sino de la capacidad de “reprogramarse” en tiempo real. El hongo, literalmente, cambia de estrategia genética al entrar en contacto con tejido humano. Y hay un detalle aún más interesante: dfl está presente en especies patógenas, pero ausente en hongos no infecciosos. Es un blanco terapéutico casi perfecto.
Una amenaza en aumento y una pista evolutiva inquietante
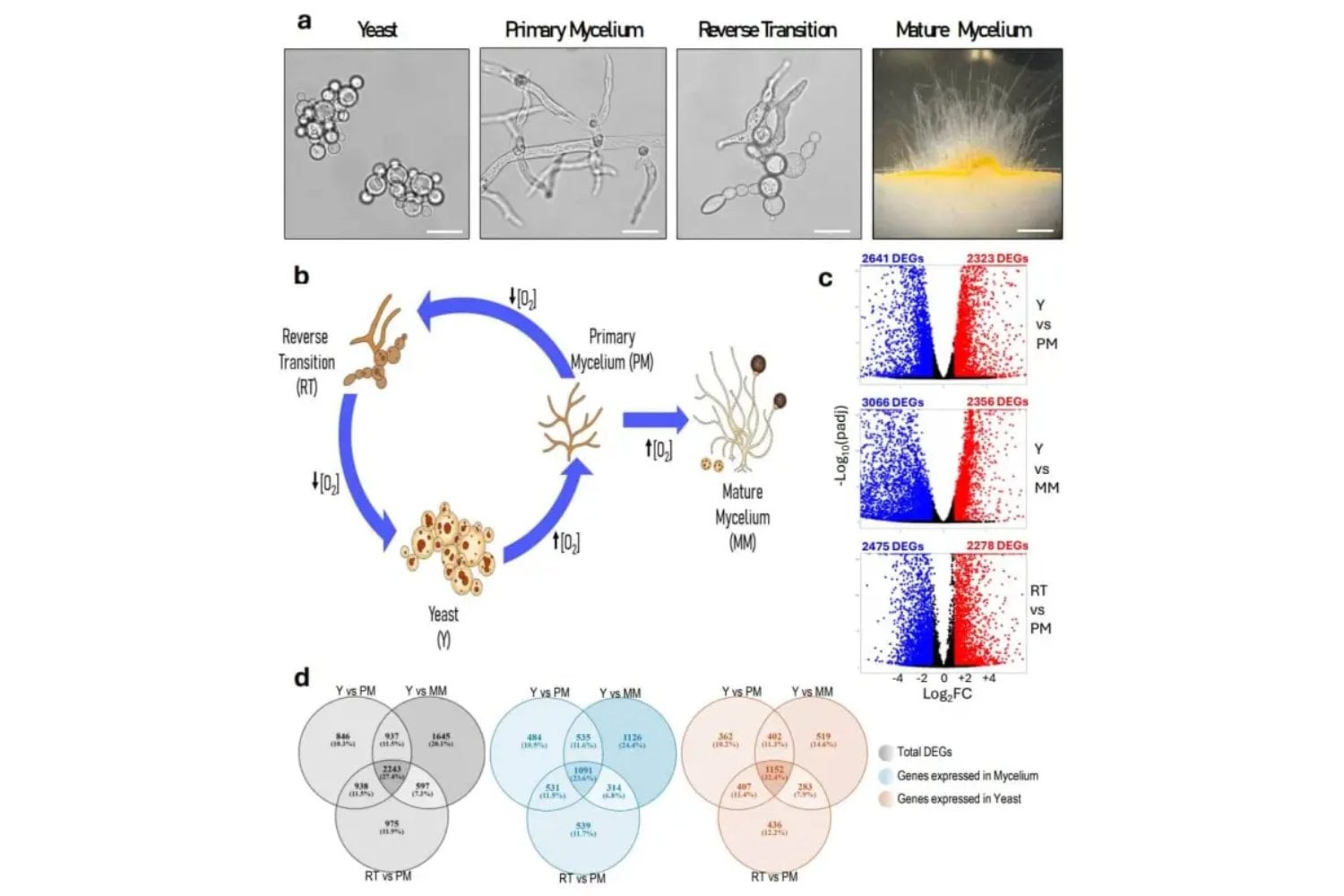
La mucormicosis, aunque considerada rara, ha mostrado repuntes preocupantes en los últimos años. Su alta mortalidad la convierte en una prioridad médica silenciosa. El estudio revela además un fenómeno de evolución convergente: distintas familias de hongos han desarrollado mecanismos similares para activar su fase patógena. No es una anomalía aislada. Es una estrategia evolutiva que ha funcionado repetidamente.
Y aquí aparece un desafío mayor: los hongos son evolutivamente más cercanos a nosotros que las bacterias. Eso hace que desarrollar antifúngicos sea complicado, porque muchos fármacos afectan también a nuestras propias células. Por eso este hallazgo es relevante. En lugar de atacar indiscriminadamente al hongo, se podría bloquear específicamente el interruptor que activa su fase infecciosa. No eliminar al organismo, sino impedir que se convierta en amenaza.
Hacia terapias antifúngicas de precisión
Conviene mantener la cautela. Estamos ante ciencia básica de alto nivel, no ante un medicamento listo para farmacia. Identificar los interruptores genéticos es solo el primer paso; convertirlos en dianas farmacológicas requiere años de desarrollo. Pero la dirección es clara: entender la arquitectura regulatoria del genoma permite diseñar estrategias más precisas y menos tóxicas.
En lugar de disparar a ciegas contra el hongo, ahora sabemos dónde está el panel de control. Y si algo demuestra este estudio es que, en biología, la diferencia entre un organismo inofensivo y una amenaza letal puede depender de un simple interruptor molecular.